Die moorLDI2-IR Laser-Doppler-Imager bieten eine gut etablierte, hochwertige Lösung zur Darstellung des Blutflusses im Gewebe für Ihre Anwendungen in der Klinik oder in der Grundlagenforschung. Das System wird routinemäßig in zahlreichen Laboratorien und Kliniken weltweit eingesetzt und vereint ein einzigartiges optisches Design mit spezieller Signalverarbeitung, um die höchste Auflösung und die schärfsten Bilder in dieser Produktklasse zu liefern.
Laser-Doppler-Imaging (LDI) wird oft mit dem Laser-Speckle-Imaging verglichen und obwohl es einige Gemeinsamkeiten gibt, bieten beide Techniken eigene Vorteile. LDI bietet generell eine höhere Eindringtiefe, die die Visualisierung von kleinen Gefäßen unter der Gewebeoberfläche erlaubt. Dies ist optimal für die Darstellung der Angiogenese oder für Messungen des cerebralen Blutflusses durch die Schädeldecke.
Der moorLDI2-IR erlaubt ebenfalls die Darstellung einer sehr großen Fläche – bis zu 50 cm x 50 cm in einem Scan. Für einige Anwendungen ist dies eine notwendige Bedingung.
Andere Funktionen und Vorteile sind:
- Berührungslose Messungen – schmerzfrei für Patienten, keine Infektionsgefahr, keine chemischen Kontrastmittel oder Farben nötig.
- Verwendung bei Raumbeleuchtung – in den meisten wissenschaftlichen, klinischen Räumlichkeiten und im OP-Bereich.
- Flexible Scangröße – von der Größe einer Fingerspitze bis zur Größe eines Oberkörpers.
- Hohe räumliche Auflösung – um die kleinsten Details bis zu 100 µm darzustellen.
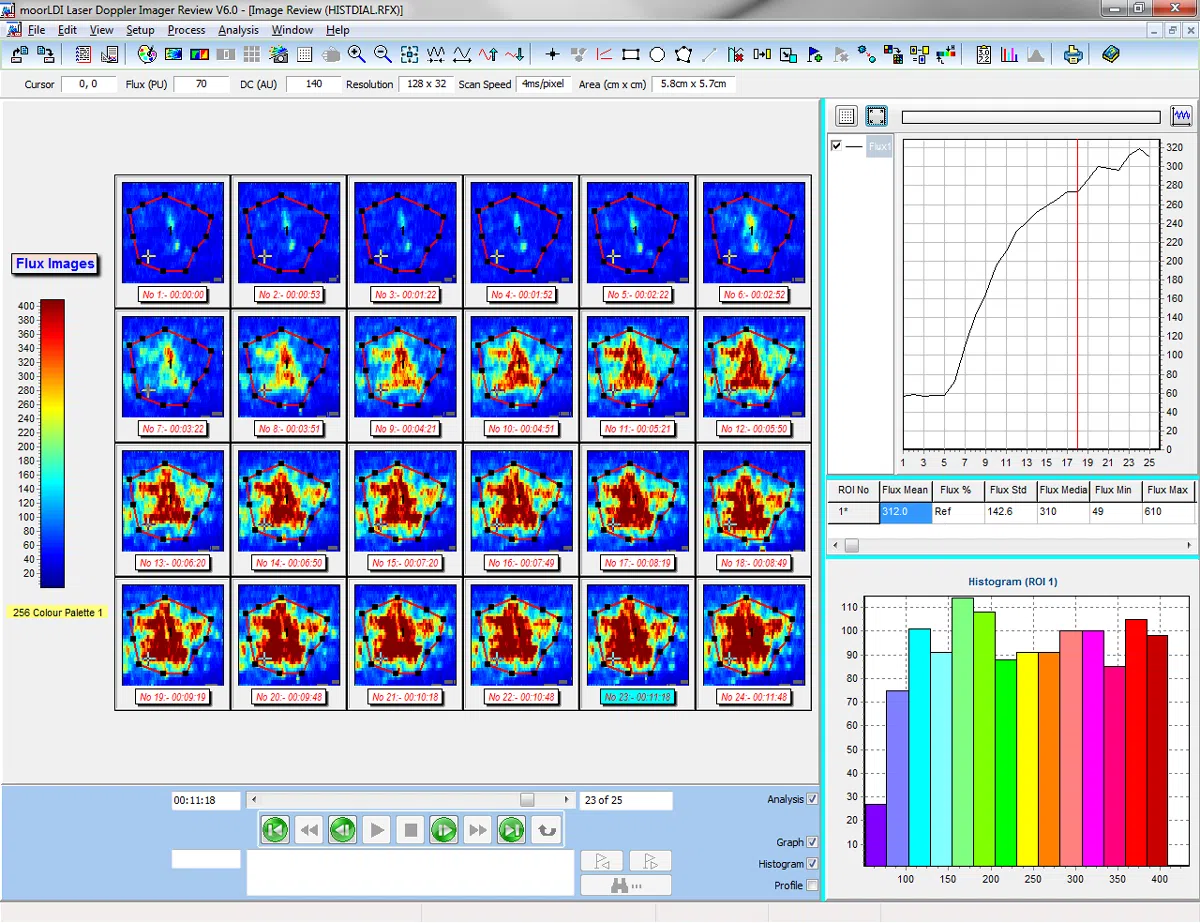
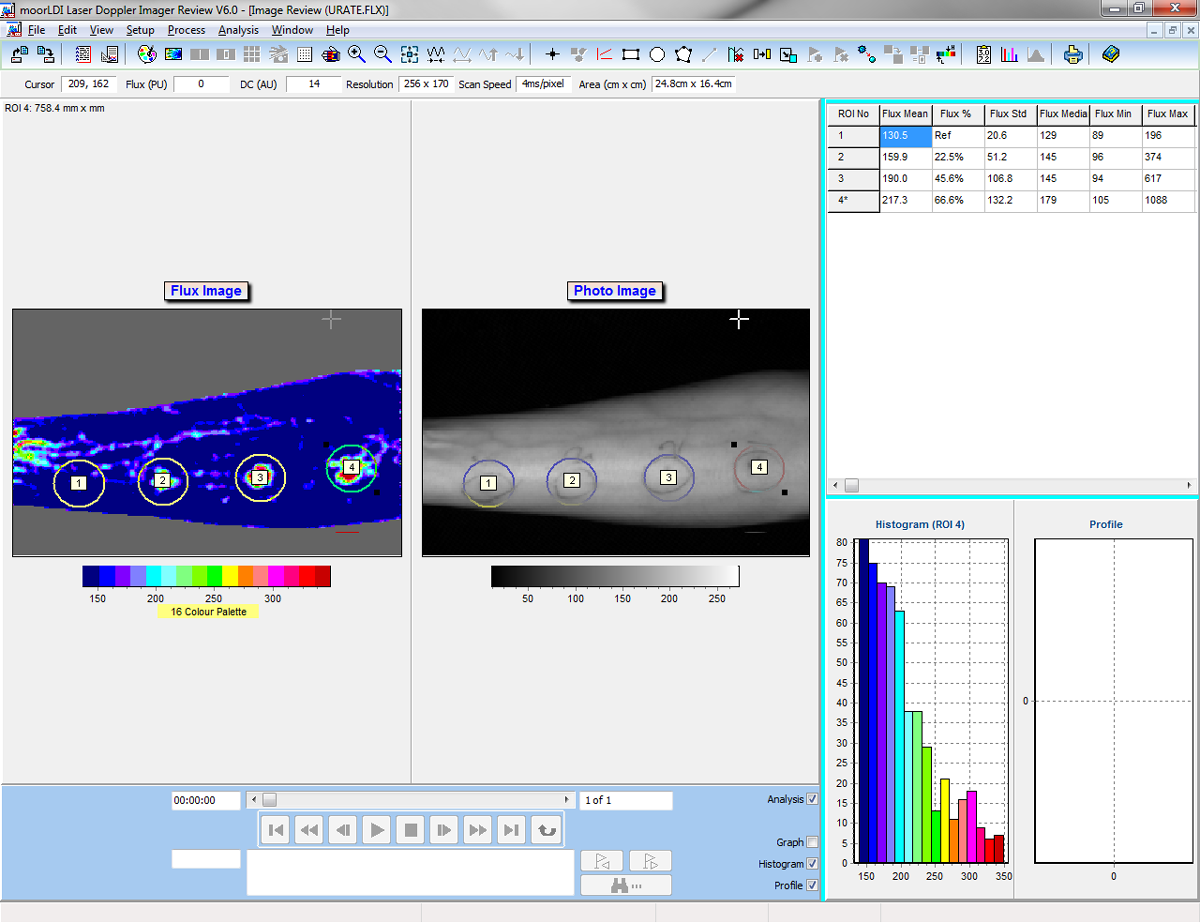
- Einzelbild und automatisierte Bildgebung – Vergleich des Blutflusses von Region zu Region innerhalb desselben Scans und wiederholtes Scannen derselben Region über längere Zeit.
- Fortschrittliche Windows-kompatible Software – diese erleichtert die Einstellungen und das Scannen. Vielseitige Analysefunktionen ermöglichen die bestmögliche Verarbeitung der erfassten Daten.
- Protokollkontrolle – Programmierung von Hitzestimulation, Druckmanschetten und transdermaler Medikamentengabe. Reproduzierbar, präzise und verlässlich.
- Digitale Trigger für Ein- und Ausgänge – zur Synchronisierung mit externen Geräten.
- Digitale Signalverarbeitung und hochqualitative Optik bieten höchste Sensitivität bei Veränderungen des Blutflusses und hervorragende Zuverlässigkeit.
- Auswahl der Laserwellenlänge – zur Messung von oberflächlichen oder etwas tieferen Gewebeschichten.
- Auswahl der Befestigung – von Tischhalterungen bis zu Rollwagen für die Verwendung im OP.